高校無機化学(非金属、金属、イオン)のまとめページ
無機化学の記事一覧。周期表と元素の分類、無機化学の勉強法もあわせて解説しています。
化学元素一覧
アルカリ金属
アルカリ土類金属
6族(クロム)
7族(マンガン)
8族(鉄)
13族(アルミニウム)
15族(窒素、リン)
16族(酸素、硫黄)
ハロゲン
希ガス
化学工業の薬品製法(接触法、オストワルト法、ハーバー・ボッシュ法、アンモニアソーダ法)
非金属元素
塩素
フッ素
酸素
硫黄
ハロゲンの酸化力 ハロゲンと水の反応から強い順を理解しよう
硫酸の性質(酸化力・脱水力・吸湿性)と接触法による製法
濃硫酸と水(動画でわかる硫酸の希釈と注意点)
アンモニアの性質と製法
硝酸(希硝酸と濃硝酸)の性質と製法
金属元素
アルカリ金属と水の反応
アルカリ金属とアルカリ土類金属の共通点と違い
両性元素(アルミニウム、亜鉛、スズ、鉛)
無機物質とイオン
気体の色、におい、重さ、水溶性、捕集法、製法
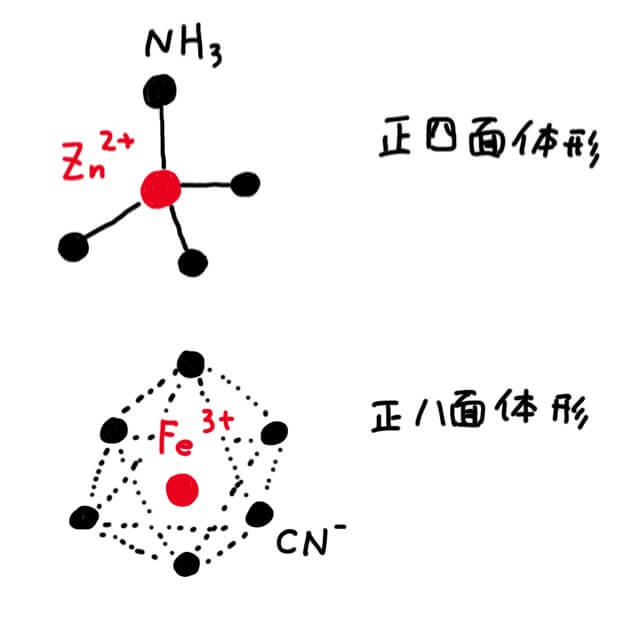
錯イオンの配位数と立体構造
ステンレス鋼、黄銅、ジェラルミンなどの合金
ここから下の解説は、無機化学を勉強するために必要なポイントです。周期表や元素の分類についておおまかに説明します。
周期表
周期表の周期は「その元素がどのように電子を持っているか」という性質を表したものです。周期は 1 から 8 まであり、すべての元素はどれかの周期に属します。
周期表の族は、元素の価電子の個数を表したもので、1 から 18 まであります。
元素は下表のように、一つの周期と一つの族に対応します。
| 元素 | 周期 | 族 |
|---|---|---|
| 酸素 | 2 | 16 |
| 銀 | 5 | 11 |
典型元素と遷移元素
元素は典型元素と遷移元素に分けられます。
- 典型元素 1~2族、12~18族
- 遷移元素 3~11族
典型元素は、価電子が化学的な性質に影響します。例えば 1 族は価電子が 1 個のアルカリ金属であり、1 価の陽イオンになりやすく、融点が低いという共通の特徴をもつ。
遷移元素は金、銀、銅などの重い金属があり、同じ周期では族が異なっても似た性質をもつことがある。
典型元素と遷移元素の違いを漠然と把握するにあたっては
- 典型元素 性質は族ごとに決まる
- 遷移元素 性質が周期ごとに決まる
と考えるとわかりやすい。
代表的な族と性質
- アルカリ金属(1族)
- アルカリ土類金属(2族)
- ハロゲン(17族)
- 希ガス(18族)
アルカリ金属は 1 価の陽イオン、アルカリ土類金属は 2 価の陽イオンになりやすく、ハロゲンは1価の陰イオンになりやすい。つまり周期表の左は陽イオン、右は陰イオンになりやすい。
18 族の元素を希ガス元素という。希ガスは反応性に乏しく、とても安定している。例えばアルゴンという希ガスは空気中にたくさん含まれていますが、私たちの体に害を与えません。
アルカリ金属とアルカリ土類金属はその水溶液が塩基性であり、ハロゲンはその水溶液が酸性です。
勉強するときのポイント
無機化学は大きく非金属元素と金属元素に分かれますが、どちらもつまるところ暗記勝負。理論化学で化学の基本を理解していれば無機化学の理論自体はそれほど難しくない。しかしその知識のボリュームはかなりのもので、高得点を狙うには知識を大量かつ正確に覚える必要があります。
また暗記一本かというとそうでもない。例えば金属イオンの分離問題はたくさんの知識を理論とひもづけてアウトプットするような応用力が試される。
高校化学は割りと「最初が難しい」学問で、多くの学生は無機化学より理論化学を苦手とする傾向がありますが、「無機化学はまあまあ好きだけど理論化学は嫌いだ」という方は無機化学を知識を入れてから理論化学を復習してもいいと思います。
高校化学を3ヶ月で習得する必殺勉強法(ある程度化学がわかる人向け。化学重要問題集を使い倒す)
私大医学部の受験前に確認するべき化学のポイント(問題形式)
元素一覧
| 原子番号 | 元素記号 | 元素名 |
|---|---|---|
| 1 | H | 水素 |
| 2 | He | ヘリウム |
| 3 | Li | リチウム |
| 4 | Be | ベリリウム |
| 5 | B | ホウ素 |
| 6 | C | 炭素 |
| 7 | N | 窒素 |
| 8 | O | 酸素 |
| 9 | F | フッ素 |
| 10 | Ne | ネオン |
| 11 | Na | ナトリウム |
| 12 | Mg | マグネシウム |
| 13 | Al | アルミニウム |
| 14 | Si | ケイ素 |
| 15 | P | リン |
| 16 | S | 硫黄 |
| 17 | Cl | 塩素 |
| 18 | Ar | アルゴン |
| 19 | K | カリウム |
| 20 | Ca | カルシウム |
| 21 | Sc | スカンジウム |
| 22 | Ti | チタン |
| 23 | V | バナジウム |
| 24 | Cr | クロム |
| 25 | Mn | マンガン |
| 26 | Fe | 鉄 |
| 27 | Co | コバルト |
| 28 | Ni | ニッケル |
| 29 | Cu | 銅 |
| 30 | Zn | 亜鉛 |
| 31 | Ga | ガリウム |
| 32 | Ge | ゲルマニウム |
| 33 | As | ヒ素 |
| 34 | Se | セレン |
| 35 | Br | 臭素 |
| 36 | Kr | クリプトン |
| 37 | Rb | ルビジウム |
| 38 | Sr | ストロンチウム |
| 39 | Y | イットリウム |
| 40 | Zr | ジルコニウム |
| 41 | Nb | ニオブ |
| 42 | Mo | モリブデン |
| 43 | Tc | テクネチウム |
| 44 | Ru | ルテニウム |
| 45 | Rh | ロジウム |
| 46 | Pd | パラジウム |
| 47 | Ag | 銀 |
| 48 | Cd | カドミウム |
| 49 | In | インジウム |
| 50 | Sn | スズ |
| 51 | Sb | アンチモン |
| 52 | Te | テルル |
| 53 | I | ヨウ素 |
| 54 | Xe | キセノン |
| 55 | Cs | セシウム |
| 56 | Ba | バリウム |
| 57 | La | ランタン |
| 58 | Ce | セリウム |
| 59 | Pr | プラセオジム |
| 60 | Nd | ネオジム |
| 61 | Pm | プロメチウム |
| 62 | Sm | サマリウム |
| 63 | Eu | ユウロピウム |
| 64 | Gd | ガドリニウム |
| 65 | Tb | テルビウム |
| 66 | Dy | ジスプロシウム |
| 67 | Ho | ホルミウム |
| 68 | Er | エルビウム |
| 69 | Tm | ツリウム |
| 70 | Yb | イッテルビウム |
| 71 | Lu | ルテチウム |
| 72 | Hf | ハフニウム |
| 73 | Ta | タンタル |
| 74 | W | タングステン |
| 75 | Re | レニウム |
| 76 | Os | オスミウム |
| 77 | Ir | イリジウム |
| 78 | Pt | 白金 |
| 79 | Au | 金 |
| 80 | Hg | 水銀 |
| 81 | Tl | タリウム |
| 82 | Pb | 鉛 |